1. Biografi
Amedeo Avogadro menjalani kehidupan yang sederhana dan berdedikasi kepada sains dan perkhidmatan awam, walaupun sumbangan saintifiknya tidak diiktiraf sepenuhnya semasa hayatnya.
1.1. Kelahiran dan Kehidupan Awal

Lorenzo Romano Amedeo Carlo Avogadro dilahirkan di Turin, Kerajaan Sardinia (kini sebahagian daripada Itali), pada 9 Ogos 1776. Beliau berasal daripada keluarga bangsawan yang terkemuka di Piedmont. Bapanya, Filippo Avogadro, adalah seorang peguam dan ahli parlimen yang memegang jawatan penting dalam Kerajaan Sardinia, manakala ibunya bernama Anna Vercellone.
1.2. Pendidikan
Avogadro menamatkan pengajian dalam undang-undang gerejawi pada usia 20 atau 21 tahun pada tahun 1796, dan kemudiannya memulakan kerjaya sebagai peguam, mengikuti jejak bapanya. Walau bagaimanapun, minatnya terhadap sains mula berkembang. Pada awal tahun 1800-an, beliau secara autodidaktik mendalami bidang fizik dan matematik, yang pada masa itu dikenali sebagai "falsafah positif". Minatnya ini membawa kepada penulisan kertas saintifik pertamanya mengenai kejuruteraan elektrik, yang diserahkan kepada Akademi Sains Turin pada tahun 1803.
1.3. Kerjaya Awal dan Aktiviti Akademik
Selepas beberapa tahun berkhidmat sebagai peguam, Avogadro mula beralih ke dunia akademik. Pada tahun 1806, beliau dilantik sebagai penolong profesor di Universiti Turin. Tiga tahun kemudian, pada tahun 1809, beliau menjadi profesor falsafah semula jadi di sebuah *liceo* (sekolah menengah) di Vercelli, di mana keluarganya memiliki harta dan tinggal. Di sinilah beliau secara aktif menjalankan penyelidikan dan pada tahun 1811, beliau menerbitkan artikel pentingnya yang bertajuk Essai d'une manière de déterminer les masses relatives des molécules élémentaires des corps, et les proportions selon lesquelles elles entrent dans ces combinaisonsEsei Mengenai Cara Menentukan Jisim Relatif Molekul Unsur Badan dan Perkadaran yang Memasukinya dalam Gabungan IniBahasa Perancis. Esei ini, yang mengandungi hipotesis Avogadro, diserahkan kepada *Journal de Physique, de Chimie et d'Histoire naturelle* milik Jean-Claude Delamétherie, sebuah jurnal Perancis, dan oleh itu ditulis dalam bahasa Perancis.
1.4. Kerjaya Pengajaran
Pada tahun 1820, Avogadro dilantik sebagai profesor fizik di Universiti Turin, yang pada masa itu merupakan ibu kota Kerajaan Sardinia yang dipulihkan di bawah Victor Emmanuel I dari Sardinia. Beliau merupakan profesor pertama bagi fizik matematik di universiti tersebut. Walau bagaimanapun, kerjayanya di Universiti Turin terganggu pada tahun 1823 apabila beliau kehilangan jawatannya akibat penglibatannya dalam gerakan revolusioner Mac 1821. Pihak universiti secara rasmi menyatakan bahawa mereka "sangat gembira membenarkan saintis yang menarik ini berehat daripada tugas mengajar yang berat, agar dapat memberi perhatian yang lebih baik kepada penyelidikannya." Meskipun demikian, beliau dipanggil semula ke Universiti Turin pada tahun 1833 dan mengajar di sana selama dua puluh tahun lagi sehingga persaraannya pada tahun 1850.
1.5. Aktiviti Politik dan Perkhidmatan Awam
Selain kerjaya akademiknya, Avogadro juga terlibat dalam aktiviti politik dan perkhidmatan awam. Beliau aktif dalam gerakan revolusioner pada Mac 1821 menentang Raja Victor Emmanuel I dari Sardinia. Beberapa sejarawan menyatakan bahawa beliau turut menaja beberapa revolusioner Sardinia. Beliau memegang jawatan yang berkaitan dengan statistik, meteorologi, dan berat dan ukuran, termasuk memperkenalkan sistem metrik ke Piedmont. Pada tahun 1848, beliau dilantik sebagai ahli Majlis Tertinggi Diraja mengenai Arahan Awam, selepas Raja Charles Albert dari Savoy memberikan Perlembagaan (Statuto Albertino).
1.6. Kehidupan Peribadi
Sedikit yang diketahui mengenai kehidupan peribadi Avogadro, yang digambarkan sebagai seorang yang bersahaja dan religius. Beliau berkahwin dengan Felicita Mazzé pada tahun 1815 dan dikurniakan enam orang anak.
1.7. Kematian
Amedeo Avogadro meninggal dunia pada 9 Julai 1856, di Turin, pada usia 80 tahun.
2. Pencapaian Saintifik
Sumbangan saintifik Amedeo Avogadro adalah asas kepada kimia dan fizik moden, terutamanya dalam memahami sifat gas dan perbezaan antara atom dan molekul.
2.1. Hukum Avogadro
Hukum Avogadro adalah pencapaian saintifiknya yang paling terkenal. Hukum ini menyatakan bahawa "isipadu gas yang sama, pada suhu dan tekanan yang sama, mengandungi bilangan molekul yang sama." Hipotesis ini dikembangkan oleh Avogadro pada tahun 1811, tiga tahun selepas Joseph Louis Gay-Lussac menerbitkan hukumnya mengenai isipadu gas yang bergabung.
Masalah utama yang cuba diselesaikan oleh Avogadro pada masa itu adalah kekeliruan yang wujud antara konsep atom dan molekul. Beliau adalah saintis pertama yang dengan jelas membezakan kedua-dua entiti ini, dengan menyatakan bahawa gas terdiri daripada molekul, dan molekul ini pula terdiri daripada atom. Sebagai contoh, John Dalton pada masa itu tidak mempertimbangkan kemungkinan ini, percaya bahawa zarah unsur adalah atom tunggal. Avogadro tidak secara langsung menggunakan perkataan "atom" tetapi merujuk kepada "molekul unsur" untuk merujuk kepada apa yang kita kenali sebagai atom hari ini. Beliau juga memberikan perhatian yang lebih kepada definisi jisim, membezakannya daripada berat.
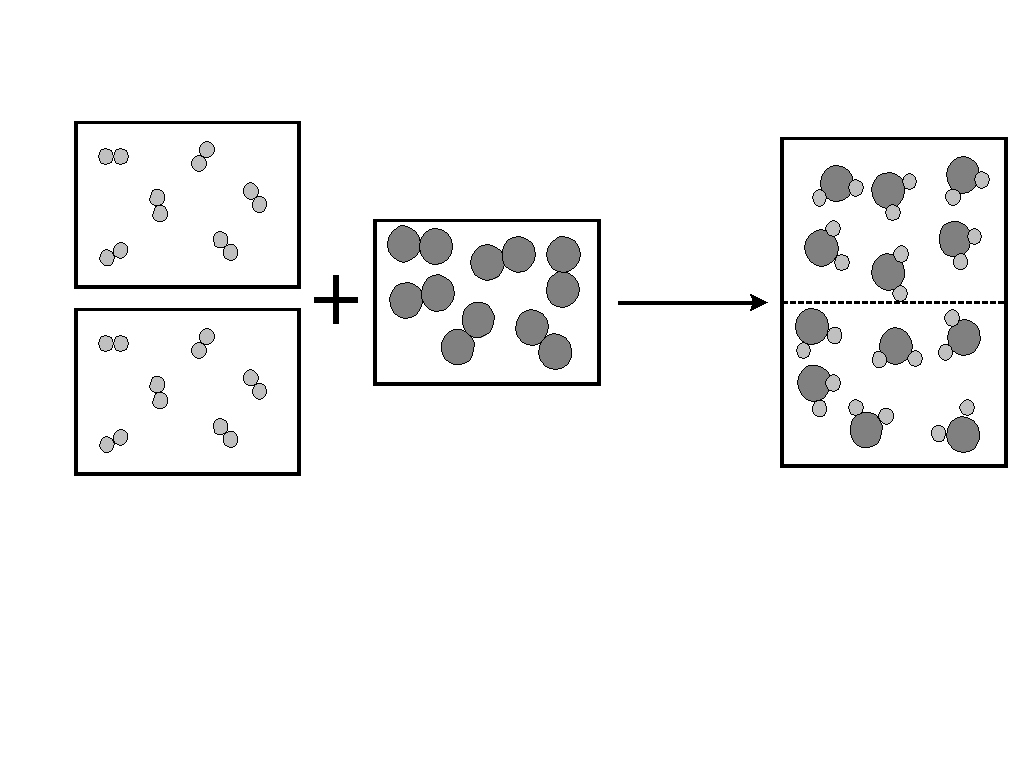
Untuk menggambarkan hukumnya, Avogadro menggunakan contoh tindak balas gas. Jika hidrogen (2 isipadu) dan oksigen (1 isipadu) bergabung untuk membentuk wap air (2 isipadu), hukum Dalton yang menyatakan H + O → HO tidak dapat menjelaskan nisbah isipadu 2:1:2 ini. Avogadro, dengan hipotesis molekul dwiatomnya, mencadangkan bahawa gas hidrogen dan oksigen wujud sebagai molekul dwiatom (H2 dan O2). Oleh itu, tindak balas yang betul adalah 2H2 + O2 → 2H2O, yang selaras dengan nisbah isipadu yang diperhatikan secara eksperimen. Hipotesis pertama Avogadro mengenai isipadu gas yang sama tidaklah revolusioner, tetapi apabila digabungkan dengan hipotesis molekul dwiatom, ia menunjukkan nilai sebenar.
Hukum Avogadro juga menyatakan bahawa pada keadaan piawai, iaitu 0 °C dan tekanan 101.30 K Pa, satu mol sebarang gas akan menduduki isipadu 22.414 L, tanpa mengira jenis gas tersebut. Hukum ini secara khususnya berlaku untuk gas ideal.
2.2. Perbezaan antara Atom dan Molekul
Sumbangan paling penting Avogadro adalah keupayaannya untuk membezakan secara jelas antara atom dan molekul. Pada zamannya, konsep ini sering kali bercampur aduk, menyebabkan kekeliruan dalam memahami tindak balas kimia. Avogadro menyatakan bahawa gas terdiri daripada molekul, dan molekul ini pula terdiri daripada atom. Sebagai contoh, beliau mencadangkan bahawa gas seperti hidrogen, oksigen, dan nitrogen wujud sebagai molekul dwiatom (H2, O2, N2), bukannya atom tunggal.
Pada tahun 1811, beliau berjaya mencadangkan formula molekul yang betul untuk air, asid nitrik, asid nitrus, ammonia, karbon monoksida, dan hidrogen klorida. Kemudian, pada tahun 1814, beliau turut mencadangkan formula molekul untuk karbon dioksida, karbon disulfida, sulfur dioksida, dan hidrogen sulfida. Selain itu, beliau menerapkan hukumnya kepada logam dan berjaya mengira berat atom untuk 17 jenis logam yang berbeza.
2.3. Pemalar Avogadro
Sebagai penghormatan kepada sumbangan Avogadro kepada teori molekul, bilangan molekul per mol suatu bahan dinamakan Pemalar Avogadro, dilambangkan sebagai NA. Nilai tepat pemalar ini ialah 6.02214076 × 1023 entiti per mol. Pemalar Avogadro adalah salah satu daripada tujuh pemalar penentu dalam SI dan digunakan secara meluas untuk mengira hasil tindak balas kimia, membolehkan ahli kimia menentukan jumlah bahan yang dihasilkan dengan tahap ketepatan yang tinggi.
Johann Josef Loschmidt adalah saintis pertama yang mengira nilai pemalar Avogadro, yang kadang-kadang dirujuk sebagai nombor Loschmidt di negara-negara berbahasa Jerman (walaupun Pemalar Loschmidt kini mempunyai makna yang berbeza).
2.4. Penulisan/Penerbitan Utama
Avogadro menghasilkan beberapa karya penting sepanjang kerjaya saintifiknya:
- 1811: Essai d'une manière de déterminer les masses relatives des molécules élémentaires des corps, et les proportions selon lesquelles elles entrent dans ces combinaisonsEsei Mengenai Cara Menentukan Jisim Relatif Molekul Unsur Badan dan Perkadaran yang Memasukinya dalam Gabungan IniBahasa Perancis, yang mengandungi hipotesis Avogadro.
- 1815: Mémoire sur les masses relatives des molécules des corps simples, ou densités présumées de leur gaz, et sur la constitution de quelques-uns de leur composés, pour servir de suite à l'Essai sur le même sujet, publié dans le Journal de Physique, juillet 1811Nota Mengenai Jisim Relatif Molekul Asas, atau Cadangan Ketumpatan Gasnya, dan Konstituen Beberapa Sebatian Mereka, Sebagai Susulan Esei tentang Subjek Yang Sama, Diterbitkan dalam Jurnal Fizik, Julai 1811Bahasa Perancis, yang membincangkan ketumpatan gas.
- 1821: Nouvelles considérations sur la théorie des proportions déterminées dans les combinaisons, et sur la détermination des masses des molécules des corpsPertimbangan Baru tentang Teori Perkadaran yang Ditentukan dalam Gabungan, dan Penentuan Jisim AtomBahasa Perancis dan Mémoire sur la manière de ramener les composès organiques aux lois ordinaires des proportions déterminéesNota Mengenai Cara Mencari Komposisi Organik mengikut Undang-undang Biasa Perkadaran Yang DitentukanBahasa Perancis.
- 1837-1841: Beliau menerbitkan karya utamanya dalam empat jilid, bertajuk Fisica dei corpi ponderabili, ossia Trattato della costituzione materiale de' corpiFizik Jasad Berat, atau Risalah tentang Konstitusi Bahan JasadBahasa Itali.
2.5. Bidang Penyelidikan Lain
Selain sumbangannya yang terkenal dalam teori molekul, Avogadro juga meneroka pelbagai bidang saintifik lain. Beliau menulis banyak kertas kerja mengenai elektrik, penyulingan cecair, haba tentu, fenomena kapilari, dan isipadu atom. Penyelidikan beliau meliputi juga pengembangan haba, meteorologi, dan metrologi.
3. Sambutan terhadap Teori dan Penilaian Semula
Teori saintifik Avogadro menghadapi penerimaan yang dingin pada awalnya dan hanya mendapat pengiktirafan meluas selepas kematiannya, melalui usaha saintis lain yang memahami dan mengesahkan kepentingannya.
3.1. Penerimaan Awal dan Pengabaian
Komuniti saintifik pada masa Avogadro tidak memberikan perhatian yang besar kepada teorinya, dan hipotesisnya tidak diterima serta-merta. André-Marie Ampère mencadangkan teori yang sangat serupa tiga tahun kemudian, pada tahun 1813, tetapi teorinya juga menerima sikap acuh tak acuh yang sama. Beberapa faktor menyumbang kepada pengabaian awal ini:
- Kesukaran Pemahaman:** Kertas kerja Avogadro, terutamanya Essai 1811, dianggap sukar difahami, mungkin sebahagiannya disebabkan oleh latar belakang undang-undangnya yang mempengaruhi gaya penulisannya.
- Percanggahan yang Ketara:** Eksperimen yang berkaitan dengan beberapa bahan bukan organik menunjukkan percanggahan yang kelihatan dengan hukumnya, menyebabkan keraguan dalam komuniti saintifik.
- Kurangnya Pengiktirafan Antarabangsa:** Avogadro kekal relatif tidak dikenali di luar Itali sepanjang hayatnya, dan beliau kurang berinteraksi secara aktif dengan ahli kimia lain di peringkat antarabangsa, malah mempunyai kebiasaan untuk mengutip dirinya sendiri dalam penerbitan.
3.2. Penilaian Semula dan Pengiktirafan
Sumbangan Avogadro mula mendapat perhatian dan pengiktirafan secara meluas selepas kematiannya, terutamanya melalui usaha beberapa saintis penting:
- Stanislao Cannizzaro:** Empat tahun selepas kematian Avogadro, pada Kongres Karlsruhe tahun 1860, ahli kimia Itali Stanislao Cannizzaro memainkan peranan penting dalam mempromosikan dan menjelaskan teori Avogadro. Beliau menerbitkan esei berjudul "Sketsa Kursus Falsafah Kimia" pada tahun 1858, yang kemudiannya diedarkan di kongres tersebut. Cannizzaro menjelaskan bahawa pengecualian yang kelihatan terhadap hukum Avogadro adalah disebabkan oleh penceraian molekul pada suhu tertentu. Beliau juga menunjukkan bahawa hukum Avogadro bukan sahaja menentukan jisim molekul tetapi juga jisim atom.
- Charles Frédéric Gerhardt dan Auguste Laurent:** Kajian mereka dalam bidang kimia organik membantu menunjukkan bagaimana hukum Avogadro menjelaskan mengapa kuantiti molekul yang sama dalam gas menduduki isipadu yang sama.
- Rudolf Clausius:** Dengan teori kinetik gas yang dicadangkan pada tahun 1857, Clausius memberikan bukti lanjut yang menyokong hukum Avogadro.
- Jacobus Henricus van 't Hoff:** Beliau menunjukkan bahawa teori Avogadro juga terpakai dalam larutan cair.
Pada tahun 1911, satu mesyuarat diadakan di Turin untuk memperingati ulang tahun keseratus penerbitan kertas klasik Avogadro tahun 1811. Raja Victor Emmanuel III dari Itali turut hadir, dan pada acara ini, sumbangan besar Avogadro kepada kimia akhirnya diiktiraf secara rasmi.
4. Impak dan Warisan
Sumbangan Amedeo Avogadro telah meninggalkan impak yang berkekalan dalam bidang sains, membentuk asas bagi pemahaman moden tentang kimia dan fizik.
4.1. Sumbangan kepada Pembangunan Saintifik
Hukum Avogadro dan konsepnya mengenai perbezaan antara atom dan molekul meletakkan asas yang kukuh bagi perkembangan teori atom-molekul moden. Beliau diiktiraf sebagai salah seorang pengasas teori ini. Penemuan beliau membolehkan ahli kimia dan ahli fizik untuk:
- Menghitung Jisim Molekul dan Atom:** Hukum Avogadro menyediakan kaedah untuk menentukan jisim molekul relatif gas dan, kemudiannya, jisim atom.
- Memahami Tindak Balas Gas:** Ia menjelaskan hubungan isipadu yang mudah dalam tindak balas gas, menyelesaikan percanggahan yang wujud dalam teori atom awal.
- Asas untuk Gas Ideal:** Hukum Avogadro menjadi salah satu prinsip asas dalam pembangunan hukum gas ideal, yang penting dalam pelbagai aplikasi saintifik dan kejuruteraan.
- Penting dalam Pendidikan Kimia:** Hukum Avogadro adalah salah satu konsep asas yang diajar pada peringkat awal pembelajaran kimia di sekolah dan universiti, kerana ia adalah kunci untuk memahami stoikiometri dan sifat gas.
- Idea Pengiraan Zarah:** Beliau memberikan idea bahawa gas boleh digunakan untuk mengira bilangan zarah, suatu konsep yang sangat penting dalam banyak bidang saintifik.
4.2. Peringatan dan Penghormatan
Sebagai penghormatan kepada sumbangan besar Amedeo Avogadro kepada sains, beberapa entiti dan tempat telah dinamakan sempena beliau:
- Pemalar Avogadro:** Pemalar asas dalam kimia dan fizik, NA, dinamakan sempena beliau.
- Avogadrite:** Sejenis mineral yang dinamakan bersempena namanya.
- Kawah Avogadro:** Sebuah kawah bulan juga dinamakan sempena beliau.